2024年成考高起点《理化综合》每日一练试题12月06日
2024-12-06 12:17:26 来源:人人学历网
2024年成考高起点《理化综合》每日一练试题12月06日,可以帮助我们积累知识点和做题经验,进而提升做题速度。通过成考高起点每日一练的积累,助力我们更容易取得最后的成功。
单选题
1、如图5-2所示,在坐标原点0处放置一电量q1=1.6×10-9C的正点电荷,在x1=4m处P点的电场强度大小E1=0.9V/m;今在x2=2m处再放置第二个点电荷q2,测得P处总的电场强度大小E2=1.8V/m,方向沿x轴负方向,则()。 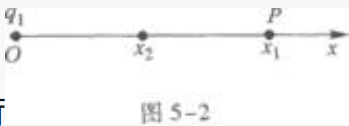
- A:q2=1.2x10-9C,正电荷
- B:q2=1.2×10-9C,负电荷
- C:q2=2.4x10-9C,正电荷
- D:q2=2.4x10-9C,负电荷
答 案:B
解 析:本题是有关电场强度概念的基本题,考查的知识点是点电荷的电场强度以及两个点电荷在电荷连线方向上电场强度的叠加。在x2处放置了点电荷q2后,P点的场强为q1、q2所产生的场强的叠加。因为电场强度是矢量,所以电场强度的叠加是矢量的合成,既要考虑大小,又要考虑方向。 为了方便起见,取坐标轴Ox的方向为电场强度的正方向,则q1产生的电场强度E1为正。设q2产生的场强为E,则由场强叠加原理知P点的总场强E2为 E2=E1+E①
由题意知,E2沿Ox轴负方向,故
E2=-1.8V/m
由式①得
E=E2-E1=-1.8V/m-0.9V/m=-2.7V/m
点电荷的场强公式是  因此q1、q2的场强分别为
因此q1、q2的场强分别为 
2、如图,用两根轻线将质量为m的重物悬挂起来,一根线保持水平,所受张力大小为T;另一根线与水平方向夹角为θ。重力加速度大小为g。则()
- A:T=mgsinθ
- B:T=mgcosθ
- C:T=mgtanθ
- D:T=mgcotθ
答 案:D
解 析:分析知,水平力T与重力mg的合力,与水平方向的夹角亦为θ,故T=mgcot0,D项正确。
多选题
1、某溶液中有NH4+、Mg2+、Al3+、Fe2+等4种离子, 若向其中加入过量的 NaOH溶液, 微热并搅拌, 再加入过量的盐酸, 溶液中大量减少的阳离子是
- A:NH4+
- B:Mg2+
- C:Fe2+
- D:Al3+
答 案:AC
主观题
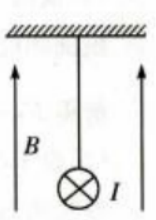
1、一绝缘细绳上端固定,下端连接在一质量m=0.08kg、长度l=0.4m的均匀金属棒中心,整个装置处在一匀强磁场中,磁场的磁感应强度大小B=0.5T,方向竖直向上,如图所示。现使一电流流过金属棒,已知电流大小I=3A,方向垂直于纸面向里,重力加速度大小g取10m/s2。求
(1)金属棒所受安培力的大小和方向。
(2)平衡后细绳中张力的大小及细绳与竖直方向夹角的正切值。
答 案:.(1)金属棒所受安培力为F=BIL=0.6N,根据左手定则知,方向水平向右。 (2)金属棒所受重力为G=mg=0.8N平衡后,安培力与重力的合力与绳中张力等大反向,设细绳与竖直方向的夹角为θ,则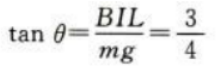 绳中张力大小为
绳中张力大小为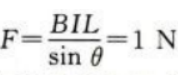
2、工业上用焙烧NaHCO3的方法生产纯碱(Na2CO3)。现有17.5g的NaHCO3样品,加热分解完全后,生成标准状况下的CO2气体2.24L。写出NaHCO3分解反应的化学方程式,计算此NaHCO3样品的纯度。
答 案:NaHCO3分解反应的化学方程式如下: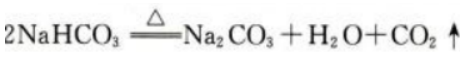 反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
反应生成标准状况下的CO2气体2.24L,其物质的量为0.1mol,故加热完全分解的NaHCO3的物质的量为0.2mol,质量为16.8g,此NaHCO3样品的质量为17.5g,所以此NaHCO3样品的纯度为16.8g/17.5g×100%=96%。
填空题
1、若要除去硫酸亚铁中含有的少量Fe3+和Cu2+,最好加入______。
答 案:铁粉
解 析:除杂质有以下要求: (1)把杂质除去或使其变成能与所需要的有效成分分离开的物质。如此题为除去FeSO4中 的Fe3+和Cu2+,加入铁粉后发生如下反应: 第一个反应把杂质(Fe3+)变成了有效成分(Fe2+),这种结果最好。第二个反应把混在溶液中的Cu2+变成了不溶于水的Cu单质,用过滤法即可与Fe2+分开。
第一个反应把杂质(Fe3+)变成了有效成分(Fe2+),这种结果最好。第二个反应把混在溶液中的Cu2+变成了不溶于水的Cu单质,用过滤法即可与Fe2+分开。
(2)不能引入新杂质。只从与Fe3+、Cu2+反应的角度看,不加铁粉加锌粉也可以。因为加锌粉后,发生如下反应: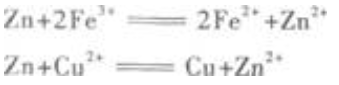 从反应方程式看,的确除去了Fe3+和Cu2+,但却引入了Zn2+,不符合要求。
从反应方程式看,的确除去了Fe3+和Cu2+,但却引入了Zn2+,不符合要求。
2、通常情况下,钠在空气中燃烧火焰呈黄色;氢气在氯气中燃烧火焰呈()色,甲烷在空气中燃烧火焰呈()色
答 案:苍白;淡蓝
解 析:根据物质的性质及实验现象可得。
简答题
1、一定质量的某铝屑和铁屑的混合物与足量稀硫酸反应后放出氢气8.96L(标准状况),同质量的此混合物与足量的氢氧化钠溶液反应,放出氢气6.72L(标准状况),求混合物中铝和铁的质量。
答 案: 答:原混合物中铝的质量为5.4g,铁的质量为5.6g。
答:原混合物中铝的质量为5.4g,铁的质量为5.6g。
2、利用氨氧化法制硝酸,试计算生产2吨60%的硝酸,需氨多少吨?(NO循环使用)
答 案:设生产2吨60%的硝酸需氨x吨,由于氨氧化法制硝酸的各步反应为 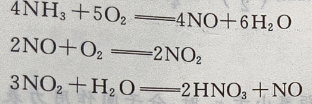 因为NO可循环使用,故简化以上关系,则得:
因为NO可循环使用,故简化以上关系,则得: